你或许听过“磷酸化”“蛋白激酶”这些听起来很“硬核”的生物学名词,但很少有人知道,它们是细胞内最精密的“信号调控师”——小到细胞的生长、代谢,大到癌症的发生、发展,都离不开它们的“操盘”。
关于磷酸化与蛋白激酶的协同调控机制,今天,我们就用通俗的语言,读懂这两个“细胞核心玩家”的故事。
先搞懂基础:什么是磷酸化与蛋白激酶?
简单来说,磷酸化就像是给蛋白质“按开关”——细胞里的蛋白质,通过添加或移除一个“磷酸基团”(相当于开关按钮),就能快速切换“激活”或“失活”状态,从而调控各种细胞功能。
而负责“按开关”的,就是蛋白激酶。它们就像细胞内的“专属电工”,专门负责给蛋白质添加磷酸基团,启动信号传导;与之对应的,还有“磷酸酶”负责“关灯”,移除磷酸基团,终止信号。一开一关之间,细胞的生长、代谢、分裂等过程就被精准调控。
更关键的是,一个蛋白激酶可以调控多个蛋白质,一个蛋白质也能被多个激酶磷酸化——这种复杂的“交叉调控”,构成了细胞内庞大的信号网络,就像一张精密的“电路网”,确保细胞各项活动有序进行。
研究新发现:磷酸化与激酶的“隐藏玩法”
过去我们对磷酸化的了解,大多局限于“单一激酶调控单一蛋白”,然而事情远比想象中复杂。
1. “信号整合者”的多重调控,藏着代谢与信号的双向奔赴
Humphrey等研究指出,细胞内存在很多“信号整合者”(比如AS160、PFK2家族、TSC等),它们能被多个不同的激酶磷酸化,从而整合不同的信号,应对不同的细胞环境。
举个例子:AS160是调控葡萄糖转运的关键蛋白,它既能被胰岛素激活的Akt激酶磷酸化,也能被运动激活的AMPK激酶磷酸化——这就解释了“为什么胰岛素和运动都能促进细胞吸收葡萄糖”,本质上是两个不同的信号,通过磷酸化同一个“整合者”,实现了功能的协同。
更有意思的是,代谢和信号是“双向奔赴”的:不仅激酶调控代谢,代谢产物也能反过来调控激酶活性。比如AMPK激酶,它能感知细胞内的能量水平,当细胞能量不足时,AMPK被激活,通过磷酸化下游蛋白,启动“节能模式”(关闭耗能的生物合成,开启产能量的分解代谢),维持细胞存活。
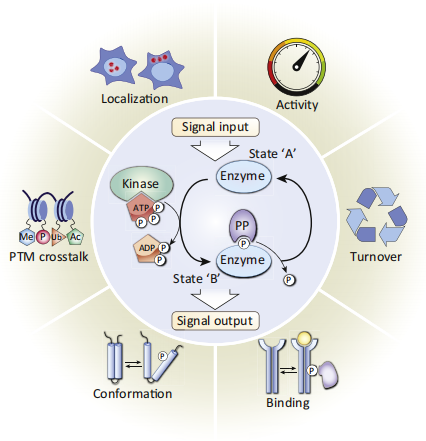
可逆蛋白磷酸化是一种分子开关机制[Humphrey,et.al]。
2:破解“黑暗磷酸化组”,找到癌症的“潜在靶点”
Jiang等聚焦于一个关键问题:细胞内有大量“未被注释”的磷酸化位点(被称为“黑暗磷酸化组”),我们不知道它们被哪些激酶调控,也不知道它们的功能——这正是癌症研究的“盲区”。
研究团队通过机器学习,构建了一个“磷酸化共调控网络(CoPheeMap)”,再结合激酶-底物预测工具(CoPheeKSA),成功“照亮”了这些“黑暗位点”。他们发现:
很多“黑暗磷酸化位点”其实是癌症相关的关键位点,它们被一些“未被充分研究的激酶”调控——这些激酶可能是癌症治疗的“新靶点”(比如CDK12,之前被忽视,现在发现它在多种癌症中异常激活,其抑制剂能抑制癌症细胞生长)。
通过这个网络,能快速找到“激酶-底物”的配对关系,比如预测出PDK1激酶能磷酸化PRKCA蛋白的Thr497位点,这一发现也得到了实验验证,为后续研究提供了明确方向。
为什么这些研究很重要?关系到每个人的健康
磷酸化和蛋白激酶的异常,是癌症发生的核心原因之一——很多癌细胞之所以会无限增殖、转移,就是因为“激酶开关”失控,导致细胞信号网络紊乱。比如我们熟悉的肺癌、乳腺癌、肝癌等,都存在特定激酶的异常激活(如CDK家族、AKT激酶)。
a揭示了磷酸化调控的新机制,让我们更清楚地理解“细胞信号如何失控导致癌症”;
b找到更多潜在的癌症治疗靶点(尤其是那些被忽视的“小众激酶”),为开发新的靶向药提供了思路;
c提供了更高效的研究工具(如CoPheeMap),能帮助科学家快速破解“黑暗磷酸化组”,加速癌症研究进程。
小磷酸,大作用
磷酸化看似是一个微小的分子修饰,却掌控着细胞的“生老病死”;蛋白激酶作为“调控者”,则是维持细胞秩序的关键。未来,或许我们能通过精准调控这些“激酶开关”,为疾病的精准治疗、基础科研的突破提供更有力的支撑。
参考文献:
Jiang, W., Jaehnig, E.J., Liao, Y. et al. Deciphering the dark cancer phosphoproteome using machine-learned co-regulation of phosphosites. Nat Commun 16, 2766 (2025). doi:10.1038/s41467-025-57993-2
Humphrey SJ, James DE, Mann M. Protein Phosphorylation: A Major Switch Mechanism for Metabolic Regulation. Trends Endocrinol Metab. 2015;26(12):676-687. doi:10.1016/j.tem.2015.09.013
