在实体瘤内部,缺氧是最普遍、最致命的微环境特征。而细胞应对缺氧的核心执行者,就是一类关键转录因子——HIF-1。它决定癌细胞的生存、代谢、血管生成、转移与耐药,是近年来肿瘤基础与转化研究的绝对焦点。今天我们用专业且易懂的方式,来拆解 HIF-1 的结构、调控、功能与临床价值。
一、HIF-1 是什么:缺氧应答的核心转录因子
HIF-1(Hypoxia-inducible factor -1,缺氧诱导因子)是bHLH-PAS 家族异二聚体蛋白,由氧敏感的 α 亚基和组成型表达的 β 亚基(HIF-1β/ARNT)组成。1992年,HIF-1 首次被鉴定为调控 EPO(促红细胞生成素)的关键蛋白;此后人们发现,它是细胞感知低氧、启动适应程序的总开关。
二、结构与亚型:三兄弟分工明确
HIF 家族共有 3 个亚型,HIF-1, HIF-2和HIF-3,其中 HIF-1α、HIF-2α 主导肿瘤进程。他们共同结构域是决定其功能的关键,包括:
bHLH:负责结合 DNA 上的缺氧应答元件(HRE)
PAS:α 亚基与 β 亚基发生异二聚化的核心结合位点
ODDD:氧依赖降解区,决定蛋白是否被降解
N-TAD/C-TAD:结合 p300/CBP 等共激活因子,启动转录
NLS:核定位信号,介导复合体进入细胞核
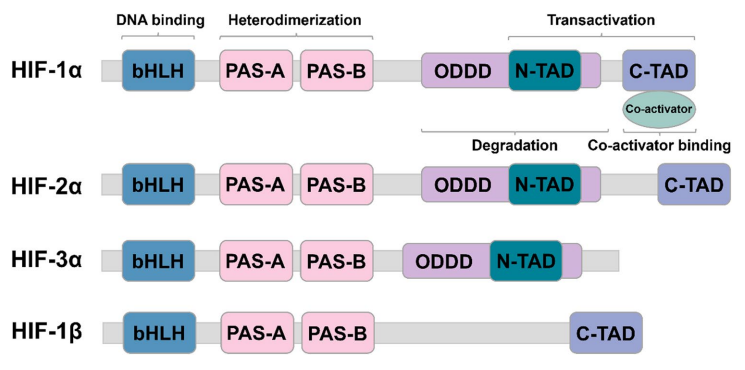
HIF 亚型结构及结构域[from Shi,et.al].
HIF 家族不同亚型关键差异
|
亚型 |
表达特点 |
核心功能 |
|
HIF-1α |
全身广泛表达 |
急性缺氧应答,主导糖酵解、细胞存活 |
|
HIF-2α |
肾、肺、血管等特异表达 |
慢性缺氧、血管重塑、干性维持、增殖 |
|
HIF-3α |
局限分布 |
负调控,抑制 HIF-1/2 活性 |
三、结合与入核:α 与 β 如何组装并进入细胞核?
HIF-1 的激活必须经历“二聚化→入核→转录”三步,这是通路最核心的分子逻辑。
HIF-1α 在细胞质稳定后,α 亚基的 PAS 结构域与 β 亚基的 PAS 结构域结合,形成稳定异二聚体。α/β亚基在细胞质完成组装后,依赖 α 亚基上的核定位信号(NLS)被核转运蛋白识别,通过核孔复合体主动转运进入核内,入核后结合 HRE 序列,启动下游几百个基因。简单来说:α 亚基负责感知缺氧、带队入核;β 亚基负责稳定结构、支持转录。想要成功启动转录,缺一不可。
四、经典调控:氧气决定 HIF-1α 的生死
HIF-1α 的核心调控逻辑非常简单,有氧被降解,缺氧即激活。
在常氧(氧气充足)条件下,PHD 酶羟基化 HIF-1α , 被 VHL 泛素化标记 ,蛋白酶体将其快速降解;FIH 进一步阻断共激活因子结合, 该通路完全沉默。在缺氧下环境中,PHD/FIH 活性被抑制 ,导致HIF-1α 无法被降解,从而在胞质内累积, 其PAS 结构域结合 β 亚基后形成异二聚体,该二聚体结合到缺氧应答元件(HRE)上,并招募 p300/CBP 等共激活因子至靶基因启动子区域,从而调控基因转录。这就是缺氧肿瘤中 HIF 持续活化的根本原因。
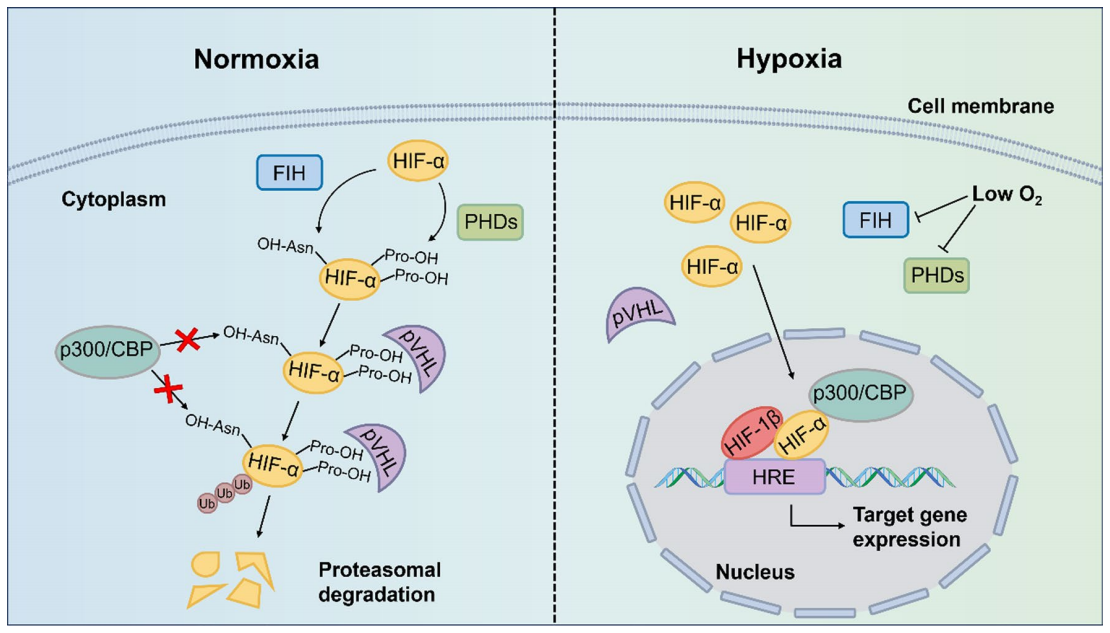
常氧与缺氧条件下HIF-α(HIF-1α/HIF-2α) 活性的经典调控[from Shi,et.al].
五、非经典调控:不缺氧也能激活 HIF
HIF 的激活并非完全依赖缺氧环境,还可通过多种非经典调控通路实现活化。近年研究发现,抑癌基因 VHL、p53 及 PTEN 的功能缺失性突变,可直接导致 HIF 蛋白稳定累积;PI3K/AKT、MAPK/ERK 等致癌信号通路的异常激活,也能显著促进 HIF 的表达与活性。同时,磷酸化、乙酰化、SUMO 化等翻译后修饰,以及最新发现的乳酸化修饰(小鼠 K644 位点、人源 K12 位点),可通过阻断 VHL 结合来增强 HIF-1α 稳定性。此外,IL-1β、TNF-α 等炎症因子也能上调 HIF 表达。这些非经典机制共同解释了部分肿瘤在非缺氧条件下仍出现 HIF 高表达的关键原因。
六、HIF 在肿瘤中做了什么?
HIF 在肿瘤进展中发挥核心调控作用,通过激活下游靶基因广泛参与肿瘤恶性生物学行为:HIF‑1α 主要介导肿瘤细胞代谢重编程,上调糖酵解关键酶与葡萄糖转运蛋白,使癌细胞在缺氧微环境中维持能量供应;同时促进血管生成相关基因如 VEGF、Ang 等的表达,驱动肿瘤新生血管形成;此外,HIF 可调控细胞运动、细胞外基质重塑及上皮‑间质转化(EMT)相关程序,增强肿瘤细胞的侵袭与转移能力;还能通过降低 DNA 损伤、上调药物外排泵、维持肿瘤干细胞特性等方式介导放化疗抵抗;并通过重塑肿瘤免疫微环境抑制免疫细胞浸润与杀伤功能,最终共同促进肿瘤的恶性演进与治疗耐受。
七、临床意义:从标志物到靶向药
在临床层面,HIF‑1α/2α 不但是重要的肿瘤预后标志物,其高表达通常提示肿瘤侵袭性更强、易发生转移且患者预后更差;同时也是极具潜力的治疗靶点,全球首个 HIF‑2α 特异性抑制剂 Belzutifan(MK‑6482)已获批用于 VHL 综合征相关肾细胞癌,多款广谱 HIF 抑制剂也处于临床早期研究阶段;而最新发现的乳酸化修饰作为代谢与缺氧通路的交叉调控点,更为肿瘤联合治疗提供了全新方向与策略。
参考文献:
1. Shi Y, Gilkes DM. HIF-1 and HIF-2 in cancer: structure, regulation, and therapeutic prospects. Cell Mol Life Sci. 2025;82(1):44. Published 2025 Jan 18. doi:10.1007/s00018-024-05537-0
2. Lima JDCC, Hooker M, Li R, et al. HIFα isoform specific activities drive cell-type specificity of VHL-associated oncogenesis. Nat Commun. 2025;16(1):9185. Published 2025 Oct 16. doi:10.1038/s41467-025-64214-3
3. Li, C., Fu, C., Zhou, W. et al. Lactylation modification of HIF-1α enhances its stability by blocking VHL recognition. Cell Commun Signal 23, 364 (2025). doi:10.1186/s12964-025-02366-x
4. Zhang M, Li L, Mao X, et al. HIF-1α Drives Cellular Senescence Via Autophagy Activation to Promote AKI-to-CKD Transition. Am J Nephrol. Published online March 16, 2026. doi:10.1159/000551542
